www.konstruktion-industrie.com
27
'22
Written on Modified on
Foba: Von Stammdaten bis Direktmarkierung, UDI-Prozess effizient und validierungsfähig digitalisieren
Die Anforderungen an Medizintechnikunternehmen im Zusammenhang mit der UDI werden (noch) nicht weniger. Da heißt es für Unternehmen, rechtzeitig strategische Entscheidungen für die Gestaltung des UDI-Prozesses zu treffen, insbesondere in Bezug auf dessen Digitalisierung. Denn die nächste Umsetzungsfrist der MDR rückt näher: Ab Mai 2023 müssen Klasse III-Produkte mit einer UDI markiert sein.

In den kommenden Jahren folgen weitere MDR-Umsetzungsfristen für den europäischen Markt. Gleichzeitig ist mit dem 24.9.2022, der letzten FDA-Frist, die Umsetzung der UDI auf dem amerikanischen Markt abgeschlossen. Die MDR-Vorgaben ähneln denen der FDA, erfordern jedoch spezifische Herangehensweisen für die Eintragung in der EUDAMED (europäische Datenbank für Medizinprodukte), die Zusammenarbeit mit den zuständigen benannten Stellen oder für die Direktmarkierung. Auch wenn die EUDAMED erst mit Zeitverzug einsatzbereit ist, ändert sich an den Fristen für die UDI-Kennzeichnung nichts.
Das UDI-System ist komplex und betrifft vom Produktdesign bis hin zum Inverkehrbringen den gesamten Prozess der Medizinprodukteherstellung. Häufig bereitet es deshalb Schwierigkeiten, Zuständigkeiten im Unternehmen abzustimmen und die Zusammenarbeit der Verantwortlichen genau zu koordinieren, etwa zwischen Prozessmanagement, Qualitätsmanagement, Datenverarbeitung, Projektleitung, Produktion.
Am Ende dieses Prozesses ist die Lasermarkierung ein entscheidender Schritt, der die Rückverfolgbarkeit jedes einzelnen Produkts und somit die Patientensicherheit in der medizinischen Praxis erst gewährleistet.
Voraussetzung dafür: Eine durchgängig fehlerfreie Datenverarbeitung und somit am Ende eine korrekte Produktmarkierung mit den UDI-Daten, die sicher und dauerhaft auslesbar sein müssen.

Wie kann man den Aufwand im Zusammenhang mit den UDI-Vorgaben dauerhaft reduzieren?
Um Abläufe effizienter zu gestalten, Prozesse zu standardisieren und Mehrarbeit zu vermeiden, kann eine Digitalisierung mittels ERP (Enterprise Resource Planning)-Software einem Unternehmen viel Nutzen bringen. Eine ineinandergreifende Datenverarbeitung kann nämlich von den Stammdaten bis hin zur seriellen Direktmarkierung alle Schritte im Unternehmen miteinander verzahnen. Auch die optimale Anbindung der Produktionstechnik an ERP-Systeme und Datenbanken ist so gewährleistet.
Digitalisierungsmaßnahmen in diesem Bereich kann man jederzeit einführen, es lassen sich sowohl bereits auf dem Markt befindliche Produkte als auch weitere UDI-Daten neu ins System integrieren. Im Hinblick auf die bevorstehende MDR können alle UDIs, die zukünftig für die EUDAMED benötigt werden, bereits vorab im ERP gepflegt werden.
Die Verarbeitung dieser Daten ist auch Grundlage für die Aufbereitung der seriellen Beschriftung für die Lasermarkierung oder die Bereitstellung der pro Teil vergebenen 2D-UDI-Codes.
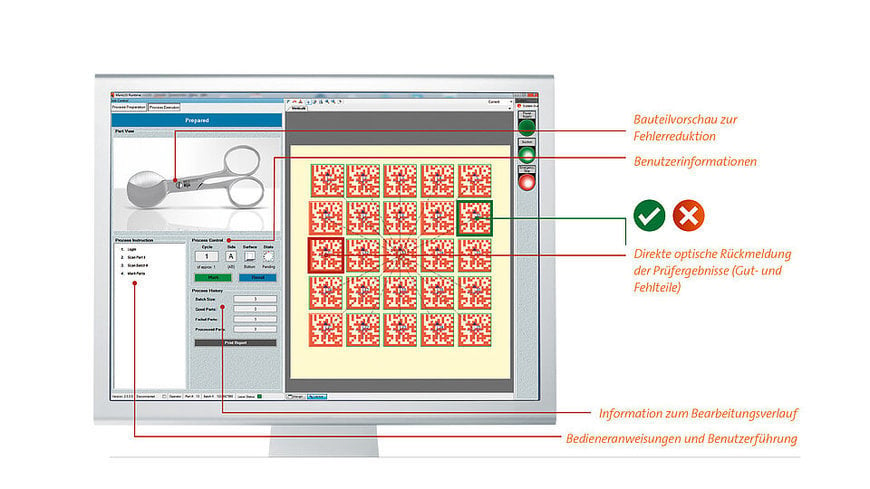
Medizinprodukt-Validierung umfasst auch die Datenintegrität
Medizinproduktehersteller sollten darauf achten, dass das verwendete ERP für die UDI- Kennzeichnung geeignet ist bzw. auch, dass die zugrundeliegenden Regularien (z. B. DIN EN ISO 13485, MDR, 21CFR820) bei der Digitalisierung berücksichtigt werden.
Vorkonfigurierte und validierungsfähige Softwarelösungen erleichtern dann nicht nur die Durchführung, sondern auch die in der Medizintechnik geforderte Validierung. Validiert wird nämlich auch die Integrität aller relevanten Daten, die wiederum zwingende Voraussetzung für Produktqualität und somit auch für Patientensicherheit ist.
www.fobalaser.com
Fordern Sie weitere Informationen an…


